近日,我院魏颢课题组在碳—金属键反应选择性调控的研究中取得了新进展,借助不同金属特有的反应活性,成功实现了多种酮类化合物高原子经济性的多样性转化,相关研究成果分别发表在中国化学会旗舰期刊CCS Chemistry和德国应用化学(Angewandte Chemie)中。
酮类结构是许多天然分子和生物活性分子中不可缺少的结构单元,也是化学合成研究中重要的反应基团,因此,酮类化合物的高效转化一直是化学家关注的重点。过渡金属催化的碳—碳活化策略近些年在酮类化合物的转化中已经取得了不错进展,但依旧存在一些亟待解决的关键问题:1. 过渡金属对羰基碳—碳键氧化加成会产生两种不同活性的碳—金属键,实现这两种键的选择性反应仍然面临巨大挑战;2. 酰基金属中间体存在可逆的羰基脱除与插入过程,而这也对两种碳—金属键活性的调整带来了困难。
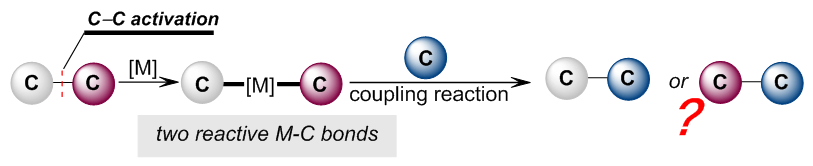
魏颢课题组长期致力于过渡金属催化羰基转化反应研究,在羰基的脱除、迁移转化中取得了原创性研究成果(J. Am. Chem. Soc. 2018, 140, 586; ACS Catal. 2020, 10, 1947),并应邀对过渡金属催化的脱羰反应进行了综述(Chem. Rev. 2020, 10.1021/acs.chemrev.0c00153)。近期,在原有工作基础上,该课题组提出了催化剂控制的羰基转化策略,以期实现对两种活性碳—金属键反应的选择性控制。
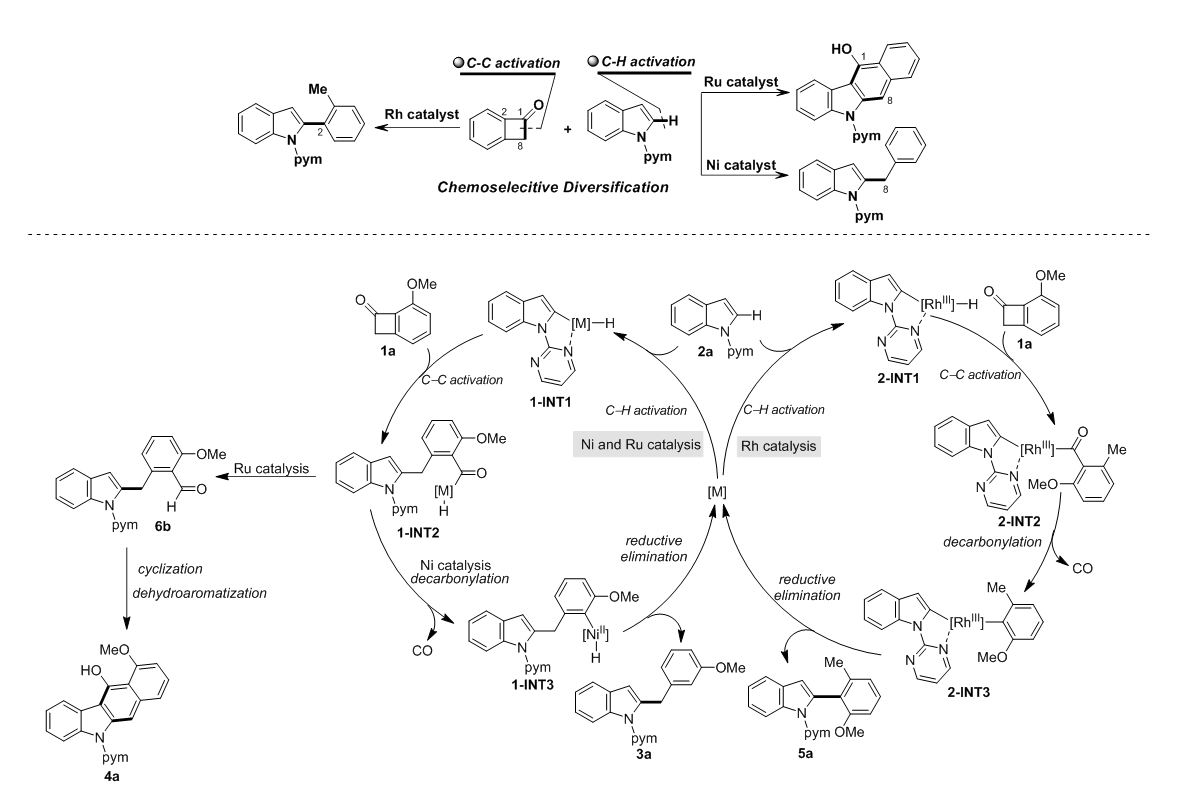
该课题组首先选用苯并环丁酮为底物,利用碳—氢活化与碳—碳活化相结合的策略,通过不同金属催化剂的选择,成功实现了苯并环丁酮向吲哚和咔唑衍生物的多样性转化:(1)当采用Ni(cod)2为催化剂时,苯并环丁酮8位碳原子与吲哚偶联,同时进一步发生脱羰,最终得到吲哚2位苄基化的产物;(2)当采用Ru3(CO)12为催化剂时,苯并环丁酮8位碳原子与吲哚偶联后未发生脱羰,羰基可以进一步参与环化构筑咔唑骨架;(3)而当采用Rh(PPh3)3Cl为催化剂时,该课题组观察到了完全不同的选择性,苯并环丁酮1位碳原子与吲哚发生偶联并进一步脱羰,最终实现了苯并环丁酮2位与吲哚的偶联,得到了芳基化吲哚。该工作通过催化剂的合理选择,不仅实现了不同碳—金属键的选择性偶联,同时也为不同活性的碳—金属键反应性的调整提供了新思路(Angew. Chem. Int. Ed. 2020, 10.1002/anie.202010244)。
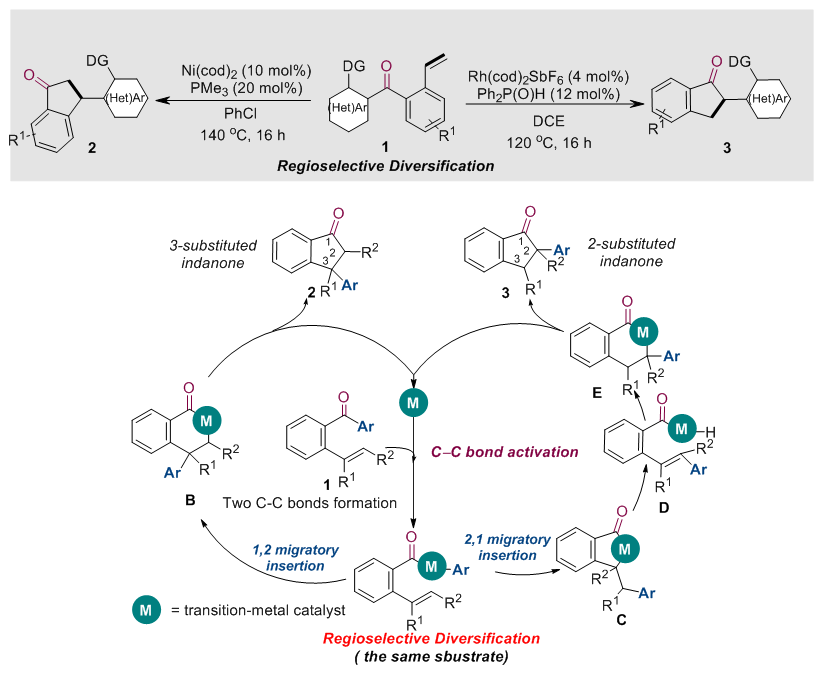
基于过渡金属催化剂在碳‒‒金属键选择性偶联中出色的调控能力,该课题组进一步探索了催化剂控制的羰基转化策略在烯烃碳酰化反应中的应用。他们采用含有末端烯烃的吲哚酮衍生物为底物,通过合理的金属催化剂选择,成功实现了催化剂控制的烯烃区域选择性碳酰化。该课题组发现,当采用Ni(cod)2为催化剂时,酰基—金属中间体会与烯烃发生1,2-迁移插入,得到3位芳基取代的茚满酮;而当催化剂调整为Rh(cod)2SbF6时,酰基—金属中间体与烯烃插入的区域选择性发生了改变,通过2,1-迁移插入最终得到了2位芳基取代的茚满酮。该工作通过催化剂控制的区域选择性反应成功实现了吲哚酮类化合物向茚满酮类骨架的多样性转化,为取代茚满酮的制备提供了一种高原子经济性的新方法(CCS Chem. 2020, 10.31635/ccschem.020.202000448)。
魏颢课题组成功报道了催化剂控制的酮类化合物多样性转化新方法,通过研究催化剂对碳—金属键反应选择性的影响,不仅有助于理解不同过渡金属催化剂在碳—碳键断裂中的特点,而且也为碳—碳键活化体系的探索开辟了新路径。