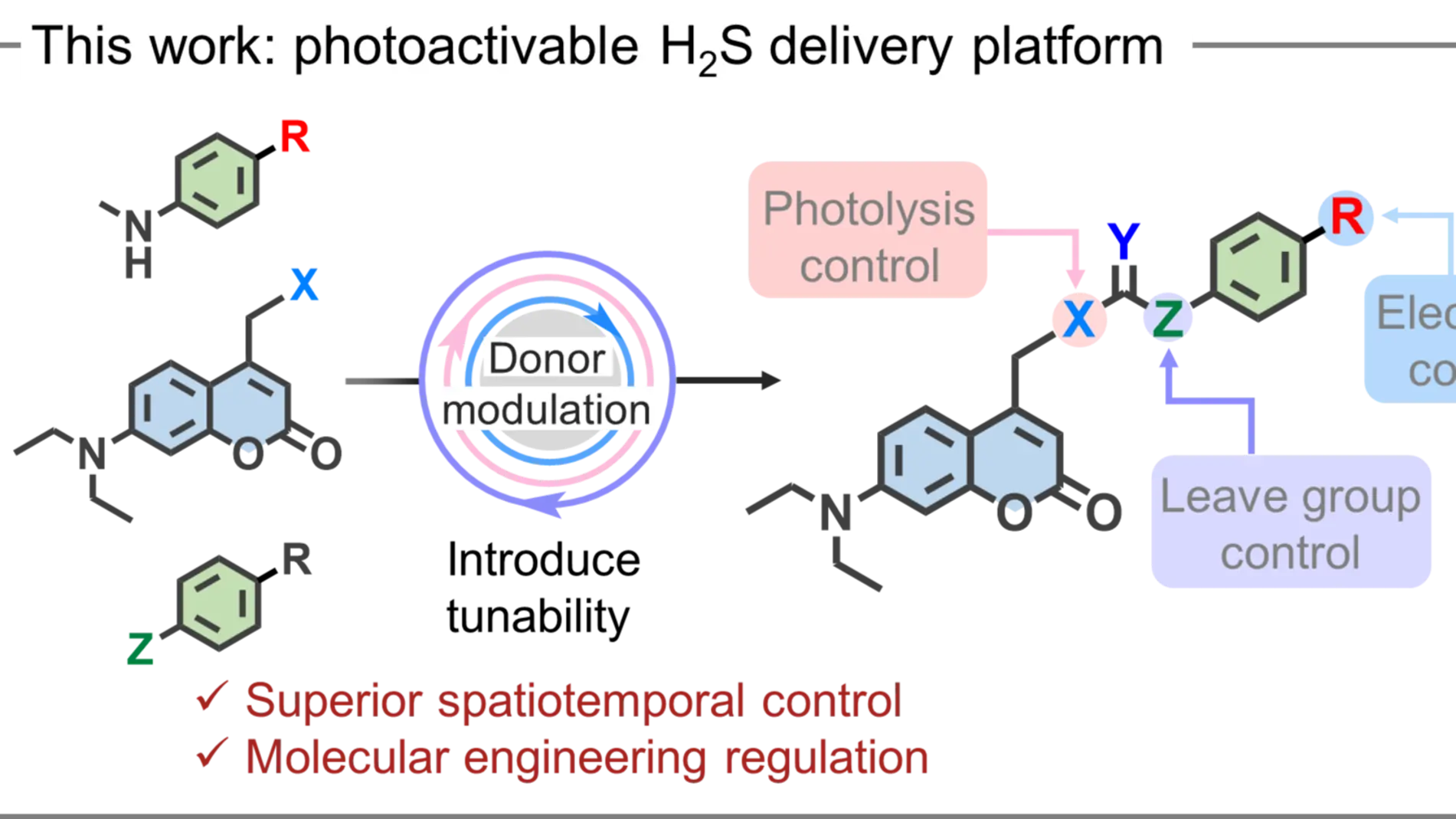
近日,张健健教授和郭媛教授合作开发了一种光响应可调控型硫化氢递送平台。研究成果以“Tunable Light-Activated Platform for Controlled Hydrogen Sulfide Release with Tracking ”为题,在化学类顶尖综合性期刊《Angewandte Chemie International Edition》上以长文(Research Article)形式在线刊发。该研究论文的第一作者和通讯作者单位均为西北大学化学与材料科学学院。原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202501685.

硫化氢(H₂S)因其组织特异性分布和多效性,使其在治疗应用中的调控变得复杂。为应对这一挑战,研究人员致力于开发能够精确调节 H₂S 浓度的供体分子,以发挥其抗炎或抗肿瘤潜力。然而,当前大多数 H₂S 供体依赖生物标志物激活,可能导致递送过程中的过早激活或耗尽,影响释放的时空精度,甚至可能加剧目标部位的病理状态。相比之下,光响应型前药或气体信使分子递送平台在控制释放方面展现出独特优势。但现有的光激活 H₂S 供体通常仅提供单一的释放曲线,难以满足日益复杂的治疗需求。因此,如何实现对 H₂S 释放曲线的精准调控,仍是当前研究的核心难题。
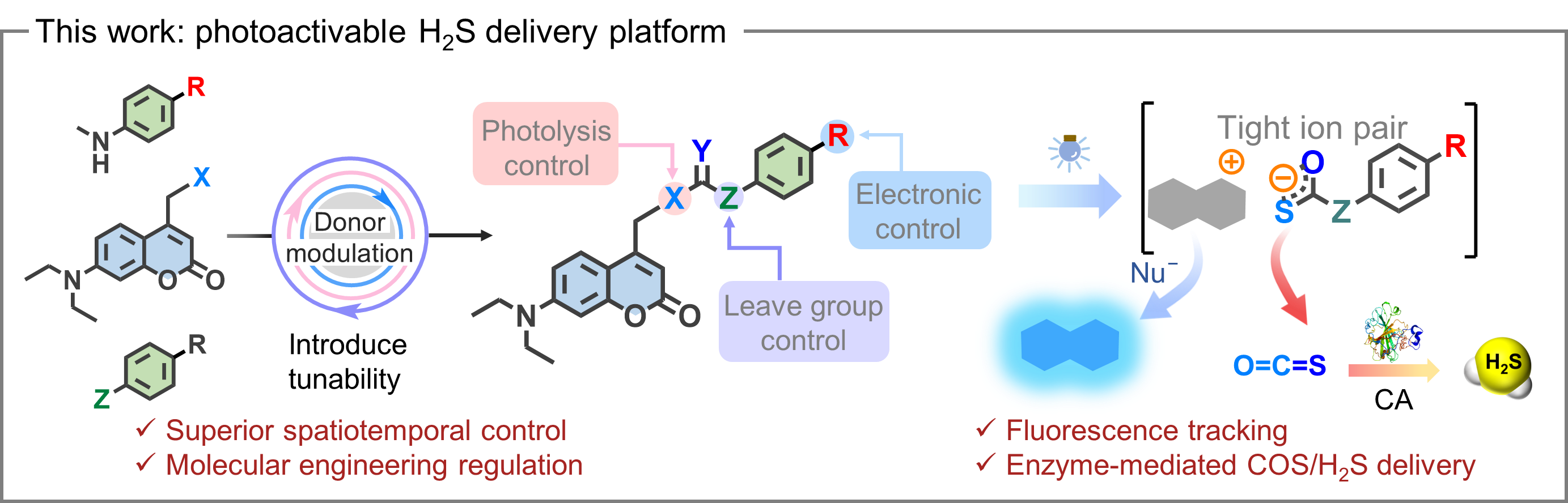
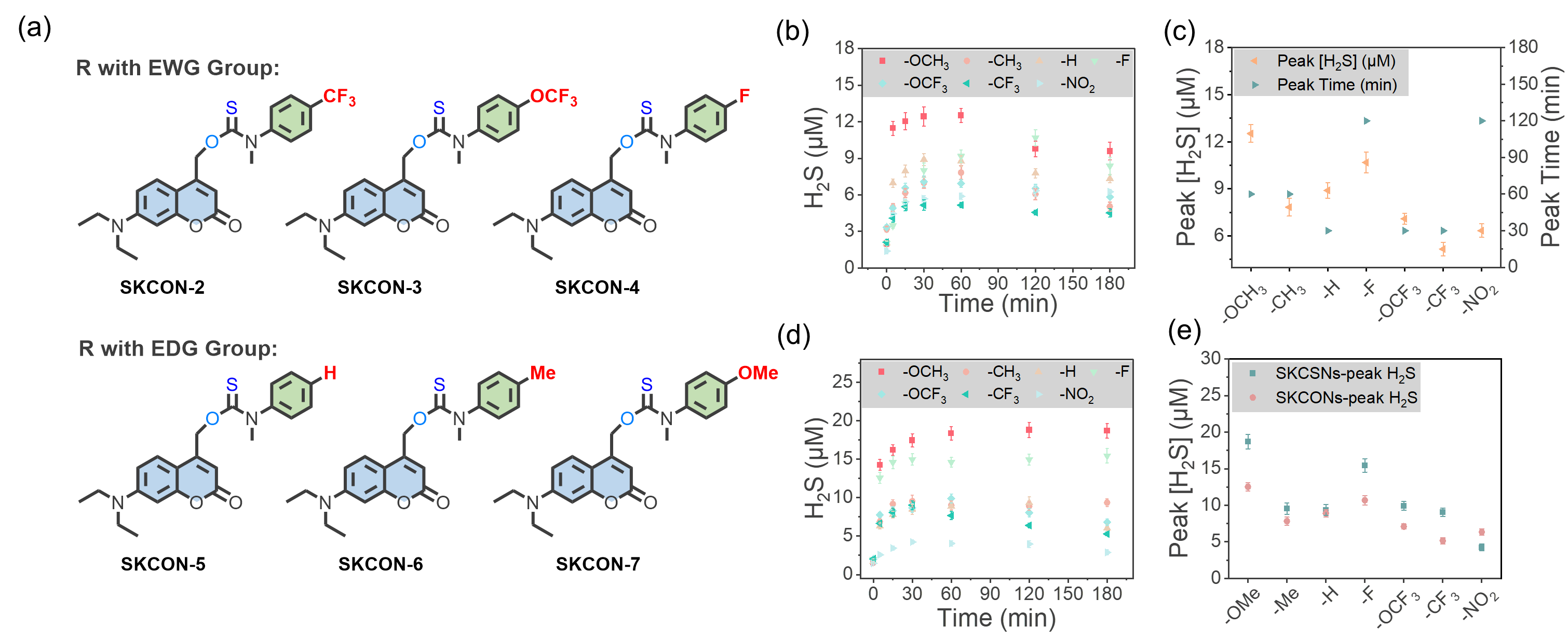
在前期研究的基础上,西北大学张健健教授/郭媛教授课题组成功开发了一种光响应可调控型硫化氢递送平台。该平台通过引入苯胺结构作为调控位点,结合供/吸电子效应和离去基团的优化选择,实现了对硫化氢释放曲线的精准调节。此外,通过调控光诱导的C-O/C-S键异裂过程,显著提升了光解效率,进一步改善了硫化氢的递送效果。研究团队在分子工程调控中发现,具有给电子效应的负载结构更有利于硫化氢的释放,其中SKCSNs类供体相较于SKCONs类供体,其释放效率得到了改善。该课题组进一步深入探究光解过程,并结合密度泛函理论(DFT)计算,成功验证了通过调控电子效应及键断裂能来精确调节硫化氢释放曲线的可行性,为相关研究提供了坚实的理论支持。
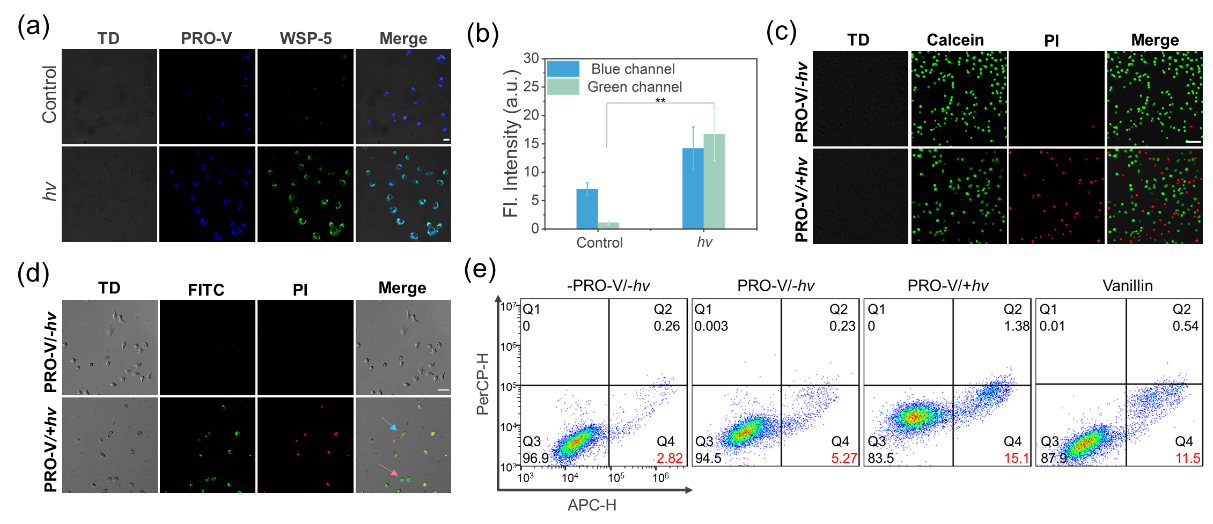
同时作者在此H₂S递送平台上成功嵌入药物分子,来构建硫化氢释放前药PRO-V,并探究了该前药用于细胞环境中COS/H₂S 和药物分子协同诱导黑色素瘤A375细胞凋亡的可行性。实验结果表明该前药分子可以实现诱导A375细胞的凋亡。
本次报道的可调控型硫化氢递送策略是在实现硫化氢可视化递送问题之后,为进一步解决硫化氢释放曲线调节的问题开展的。该平台的开发弥补了前期工作释放曲线单一的问题,同时保留了可视化递送的优势,进一步实现递送的可控可视及精细化递送。这些重要进展将显著拓展H₂S供体的分子设计空间,有望推动新型H₂S杂化前药体系的创新发展,并为其临床转化应用奠定坚实基础。